- Списание
- NB!
- Новые правила выписки рецептов на медизделия
- Сроки перехода на маркировку лекарственных препаратов
- Что нужно знать о маркировке
- Перенос сроков маркировки
- Запуск маркировки для остальных лекарств
- Что представляет собой код маркировки?
- Какое оборудование понадобится для работы
- Как должна работать система мониторинга
- Ответственность за нарушение требований к маркировке с 1 декабря 2021 года
- Маркировка лекарственных препаратов
- Сроки маркировки лекарств
- В маркировке товаров участвуют
- Алгоритм работы с маркированными лекарственными препаратами следующий
- Как подготовиться к работе с маркировкой
- Штрафы за отсутствие маркировки
- Подключитесь к системе маркировки самостоятельно
- О чём эта статья
- Алгоритм перехода на электронный документооборот
- Этап 1. Выбрать оператора ЭДО и заключить договор
- Этап 2. Провести работу с контрагентами
- Этап 3. Протестировать процессы
- Освобождение от маркировки одежды, изготовленной ремесленниками
- Эксперимент по маркировке антисептиков
- Новые сроки выдачи лицензии производителям
- Работайте с нами
- Видео
- Производители
- Дистрибьюторы
- Аптеки
- Медицинские центры
- Уведомительный режим маркировки может стать бессрочным
- Без чего не обойтись предпринимателям при торговле маркированными лекарственными препаратами
- Штрафы до 300 000 ₽ за лекарства без маркировки
- Питание для спортсменов и бытовая химия в аптеках
- Обязательный ЭДО в маркировке молочной продукции
- Процесс регистрации в системе маркировки
- Применение 1С-ЭДО при операциях с маркированными товарами
- Ответственность участников рынка
- В России упростили систему маркировки лекарств из-за повышенного спроса
- Отсрочка обязательной маркировки велосипедов
- Маркировка лекарств в 2021 году
- Какие лекарства подлежат маркировке
- Как производителю работать с маркировкой
- Как происходит процесс оборота лекарств
Списание
Списание товаров проводится через регистратор выбытия. Для этого следует считать код на упаковке в момент выдачи пациенту, а затем направить его в систему маркировки.
Таким образом, обязательная маркировка лекарств осуществляется один раз, в момент производства препаратов. Присвоенный заводом-изготовителем код является эффективным инструментом контроля движения товара от производителя к конечному потребителю, а также гарантией качества и оригинальности лекарственного препарата.

NB!
Коллеги, так же обратите внимание на документы прикрепленные к этой статье. Вы можете, как оформить конкретный недостающий документ, так и комплексно обновить докуметацию, СОПы и другую рабочую документацию для фармацевтической организации с учетом последних изменений в законодательстве.

Задайте свой вопрос экспертам МедИнфо24 там, где вам удобно:

+7 (904) 866-01-00
Новые правила выписки рецептов на медизделия
В середине месяца Министерство здравоохранения представило для общественного обсуждения проект нового порядка назначения медицинских изделий и форм рецептурных бланков на медицинские изделия, правил их оформления, а также учёта и хранения.
По замыслу Минздрава правила должны будут вступить в силу со следующего года. Новый документ содержит большое количество изменений в сравнении с действующим сейчас приказом № 1181н — подробнее о них читайте в нашем материале.
Отдельно стоит упомянуть поправку, которая коснётся не только медицинских работников, но и сотрудников аптек. В новом документе министерство обяжет аптеки хранить в течение трёх лет рецепты, предназначенных для граждан, имеющих право на бесплатное обеспечение медицинскими изделиями, в графе «Процент оплаты пациентом» которых имеется отметка «Бесплатно». Сейчас, напомним, обязанности хранить рецепты на медицинские изделия у аптек нет.
Сроки перехода на маркировку лекарственных препаратов
- С 1 июля 2019 года – начало регистрации аптек, аптечных сетей и медицинских организаций в системе «Честный знак» для работы с препаратами из перечня высокозатратных нозологий.
- С 1 октября 2019 года – введена обязательная маркировка для препаратов из перечня высокозатратных нозологий.
- С 1 июля 2020 года – началась обязательная маркировка всех лекарственных препаратов и обязательная передача сведений по ним в систему маркировки «Честный знак».
Что нужно знать о маркировке
С помощью маркировки государство контролирует оборот товаров. Уже действует маркировка лекарств, табака, одежды и текстиля, легкой промышленности, шин, парфюмерии, фототехники, обуви, молочной продукции и упакованной воды. К 2024 году планируют промаркировать все основные потребительские товары, которые производят в России или импортируют в страну.
Отсканировав код на упаковке товара, покупатель сможет удостовериться, что не купил подделку. Чтобы эта информация дошла до конечного потребителя, передавать ее друг другу и в Честный ЗНАК должны все участники оборота: производители, дистрибьюторы, торговые точки.
Вот как это работает.

Перенос сроков маркировки
В июне 2020 года Госдума приняла поправки к закону «Об обороте лекарственных средств». Законопроект о внесении поправок принят во втором чтении. Новая редакция дает Правительству возможность переносить даты маркировки лекарств.
Поправки касаются препаратов, выпущенных с 1 июля по 1 октября 2019 г. Кроме нанесения кодов, препараты нужно будет вносить в реестр. Также поправки регламентируют создание базы пациентов, которые получают лекарства на льготной основе.
До 1 января 2021 г. в Россию разрешено ввозить немаркированные препараты из-за рубежа. Но в список исключений попадают жизненно необходимые средства, выпущенные до 1 октября 2020 г. Решение в каждом случае принимает Правительство.
До 1 октября не действуют санкции для участников рынка, которые не подключились к системе мониторинга. Поэтому нельзя сказать, что произошел перенос маркировки лекарств на 2021 год. Указанный срок меньше, чем полгода.

Запуск маркировки для остальных лекарств
В законе № 61-ФЗ, который регулирует обращение лекарственных средств, указано, когда ввели маркировку для остальных лекарств — 1 июля 2020 года. И с этой даты маркировать стали уже все лекарственные средства.
Был перенос срока: изначально запуск маркировки лекарств планировался 1 января 2020 года. Однако с этой даты ввели лишь обязанность по регистрации в системе мониторинга всех участников рынка. И сделать это необходимо было до 29 февраля. Новым участникам рынка после этой 29 февраля давалось 7 дней с даты начала деятельности, чтобы пройти процедуру регистрации.
Что представляет собой код маркировки?
При маркировке лекарств используется электронно-цифровой формат Data Matrix, когда каждой упаковке присваивается двумерный код длиной в 83 символа. Специфическая структура и неповторимые комбинации знаков исключают подделки и имитации. Если в торговую сеть поступает контрафакт, система тут же распознаёт поддельное лекарство по неправильному коду и сообщает об этом. По этой причине нельзя в процессе реализации заменить какой-либо препарат таким же препаратом из другой партии, или аналогом другого бренда.
Data Matrix содержит следующие обозначения:
- «01» плюс 14 знаков – международная кодировка;
- «21» плюс 13 знаков – серийный номер продукции (генерирует оператор системы);
- «91» плюс 4 знака – проверочный ключ;
- «92» плюс 44 знака − проверочный код.
Размер маркировки на упаковке может быть разным. Чаще всего это габариты 16х16 мм, но встречаются и коды 10х10 и 12х12 мм. При формировании укрупнённых партий на поддонах, паллетах, в коробках используют кодировку GS1 128. При наведении сканера такая маркировка показывает сведения обо всех лекарственных препаратах и их количестве в упакованной таре.

Какое оборудование понадобится для работы
На полную отмену проекта не стоит надеяться. Внедрение системы учета выгодно государству. Эксперты считают, что проект будут переносить, пока рынок не адаптируется к новым условиям. Всем участникам рынка рано или поздно понадобится оборудование для чтения маркировки.
Для чтения двумерных штрих-кодов DataMatrix понадобятся:
- стационарные 2D сканеры — для продажи на кассе;
- ручные 2D сканеры — для работы на кассе и на складе;
- терминалы сбора данных — мини-компьютеры для складского учета.
Компания MERTECH выпускает 2D сканеры и ТСД, разработанные специально для системы «Честный Знак». Модели успешно прошли проверку по считыванию маленьких штрих-кодов с упаковок лекарств. Оборудование считывает информацию за доли секунды, распознает поврежденные и нечеткие коды.

Как должна работать система мониторинга
Обязательная маркировка лекарств началась 4 февраля 2015 г. , когда о новой системе впервые заговорили. Но 5 лет оказалось недостаточно, чтобы перевести рынок на новую систему работы. Государство несколько раз было вынуждено перенести сроки реализации проекта.
На каждом этапе маршрута необходимо считывать штрих-коды с упаковок лекарств. Для контроля товарооборота используются 2D коды DataMatrix. В каждом штрих-коде зашифрована уникальная последовательность данных. Этикетка содержит информацию о производителе, сроке годности препарата, уникальный номер упаковки.
Ответственность за нарушение требований к маркировке с 1 декабря 2021 года
В настоящее время за нарушение порядка работы с маркируемым товаром предусмотрена административная ответственность. В частности, за производство товаров и продукции без маркировки или с нарушением порядка маркировки (кроме алкогольной и табачной продукции) установлен штраф (с конфискацией) (ч. 1 ст. 12 КоАП РФ): для должностных лиц — в размере от 5 000 до 10 000 руб. ; для юридических лиц — от 50 000 до 100 000 руб.
За продажу товаров и продукции без маркировки, а также хранение, перевозку или приобретение таких товаров и продукции в целях сбыта (кроме алкоголя и табака) установлен штраф (с конфискацией) (ч. 2 ст. 12 КоАП РФ): для должностных лиц — от 5 000 до 10 000 руб. ; для юридических лиц — от 50 000 до 300 000 руб.
С 01. 2021 вступают в силу изменения в КоАП РФ и УК РФ, которые устанавливают новые меры административной и уголовной ответственности за нарушение правил работы с товарами, которые подлежат маркировке по законодательству РФ (Федеральные законы от 11. 2021 № 204-ФЗ, от 01. 2021 № 293-ФЗ).
В частности, установлен штраф за непредставление (неполное, недостоверное представление) сведений о маркируемых товарах в ИС МП «Честный знак» (новая статья 15. 1 КоАП РФ): для юридических лиц — от 50 000 до 100 000 руб. ; для должностных лиц — от 1 000 до 10 000 руб. Подробнее см. в № 10 (октябрь), стр. 8 «БУХ. 1С» за 2021 год и в статье «Уголовная и административная ответственность за нарушение требований к маркировке».
1С:ИТС
О мерах административной ответственности за нарушение установленных правил маркировки, что нужно сделать, чтобы снизить риск привлечения к ответственности, см. в разделе
«Консультации по законодательству»
Об уголовной ответственности в соответствии с Федеральным законом от 01. 2021 № 293-ФЗ см.
в этом же разделе
От редакции. Полезные материалы о маркировке товаров можно найти на сайте БУХ. В 1С:Лектории регулярно проводятся лекции по вопросам обязательной маркировки различных товаров, поддержке в 1С с участием представителей Центра развития перспективных технологий (ЦРПТ, оператора системы маркировки) и экспертов 1С. 2021 приглашаем на онлайн-лекцию «Маркировка упакованной воды в программах «1С:Предприятие». Подробнее см. на странице 1С:Лектория.
Маркировка лекарственных препаратов
Эксперимент по маркировке лекарственных препаратов начался еще в 2017 году. Уже с 2020 года все лекарства подлежат обязательной маркировке.
Цель такого нововведения — обеспечить рынок только качественными лекарствами, проконтролировать движение медикаментов, которые приобретаются на государственные средства, а также оперативно планировать лекарственные резервы.
Расскажем, как с ней работать.
Сроки маркировки лекарств
Необходимость маркировки лекарств установлена законом 425-ФЗ, который внес изменения в закон «Об обращении лекарственных средств». Согласно документу, каждая упаковка с лекарством должна быть промаркирована средством идентификации. Таким средством является двумерный код Data Matrix. С его помощью можно узнать основную информацию о самом лекарстве и его производителе. Каждый участник оборота лекарств считывает код специальным сканером и передает в систему Мониторинга движения лекарственных препаратов (МДЛП) сведения о том, на каком этапе оборота находится товар. Таким образом, маркировка и мониторинг движения лекарственных препаратов являются основными инструментами системы.
Этапы введения маркировки поделены на такие сроки:
- С 1 января до 29 февраля 2020 года все участники оборота лекарств должны были пройти регистрацию в системе маркировки.
- До 15 февраля 2020 года медицинские учреждения и аптеки должны были подать заявку на получение регистратора выбытия.
- До 1 мая 2020 года производители и импортеры лекарств обязаны подать заявку на получение регистратора эмиссии.
- С 1 июля 2020 года все участники оборота должны передавать сведения о движении лекарств в систему маркировки.
- С 24 октября 2020 года действует уведомительный режим маркировки, то есть аптеки могут продавать некоторые медикаменты без идентификации, если есть разрешение от Росздравнадзора.
Важно
Лекарства, произведенные до 1 июля 2020 года, маркировать не нужно.
В маркировке товаров участвуют
Регистрируют произведенные лекарства, отчитываются о введении нового кода в оборот.
Дистрибьюторы или оптовые представители
Регистрируют получение препарата и передачу его далее по цепочке.
Фиксируют прием препарата от дистрибьютора и продажу на кассе.
Отмечают поступление препарата от дистрибьютора и списания для оказания услуг.
Комментарий специалиста Евгения Мео.
Существуют две схемы приемки маркированных лекарств — прямая и обратная. При прямой схеме акцептования дистрибьютор отправляет сведения в ФГИС МДЛП об отгрузки, а розница подтверждает. При обратной покупатель лекарственных средств передает данные в ФГИС МДЛП о приемке кодов маркировки, а дистрибьютор их подтверждает.
Приемка может проходить как через товаро-учетную систему, так и в ручном режиме.
Алгоритм работы с маркированными лекарственными препаратами следующий
- Производитель получает коды маркировки лекарственных препаратов от ЦРПТ и наносит их на упаковку.
- Дистрибьютор подтверждает получение списка кодов с упаковок при отгрузке товара.
- При прямой схеме поставки поставщик передает аптеке товар вместе со списком кодов. Аптека сверяет коды со списком дистрибьютора на упаковках самостоятельно и акцептует их.
- При обратной схеме аптека сканирует код каждой упаковки при приемке и отправляет на сверку поставщику. Поставщик акцептует коды с ФГИС
- При продаже конечному покупателю провизор сканирует код маркировки на упаковке,а оператор фискальных данных отправляет его в систему МДЛП. Код выбывает из оборота.
Чтобы участники фармацевтического рынка успели полностью подготовиться к обороту медикаментами по новым правилам, Правительство внесло в программу перехода ряд изменений.
Постановление Правительства от 2 ноября 2020 года №1779 упростило порядок работы с системой мониторинга движения лекарств. Так до 1 июля 2021 года аптеки и медицинские учреждения могут выводить лекарственные препараты из оборота сразу после подачи в систему «Честный ЗНАК» уведомления об их поступлении. Кроме того, были введены упрощённые механизмы «обратной приёмки лекарственных препаратов» при их ввозе в Россию, а также при обороте внутри страны. До 1 июля 2021 года участники оборота могут оприходовать и осуществлять дальнейшие операции с лекарствами, не дожидаясь подтверждения о приёмке лекарств от поставщиков, а импортёры — ввозить лекарства, не дожидаясь подтверждения от владельцев (держателей) регистрационного удостоверения.
До 1 февраля 2021 года действовал установленный Постановлением №1779 упрощённый порядок оборота медикаментов. Производители должны были наносить на упаковку код маркировки, который сканировался аптекой на кассе. При этом дальнейшие операции с медикаментами никак не ограничивались, если система маркировки не отправляла в течение 15 минут ответ об успешной обработке данных.
В начале 2021 года были введены послабления для препаратов, выпущенных в оборот до 1 февраля 2021 года (Постановление Правительства от 28 января 2021 года № 60). Для них уведомительный характер маркировки сохранится и останется актуальным вплоть до окончания срока годности лекарств.
Как подготовиться к работе с маркировкой
Рассказываем, что значит обязательная маркировка изделий и кто станет участником процесса.
Всем участникам оборота лекарств необходимо зарегистрироваться в системе маркировки.
- Усиленная квалифицированная электронная подпись. Нужна для регистрации в ИС МДЛП всем участникам оборота лекарств.
- Электронный документооборот. Необходим на каждом этапе оборота ЛС для передачи кодов маркировки.
- Подключение к ОФД и онлайн-касса с обновленной прошивкой. Потребуется тем, кто принимает платежи наличными и банковской картой. В первую очередь это касается аптек и медицинских учреждений.
- Регистратор эмиссии. Необходим производителю и импортеру для получения кодов маркировки.
- Принтер этикеток. Необходим производителю и импортеру для нанесения кодов на упаковку.
- Регистратор выбытия. Используется в аптеках и медицинских учреждениях при продаже конечному потребителю для вывода товара из оборота.
- 2D-сканер. Нужен для считывания кодов маркировки при приёмке и продаже лекарств.
- Терминал сбора данных. Поможет ускорить инвентаризацию на складах.
- Товароучетная система, готовая к работе с маркировкой. Интеграция товароучетной системы с ИС МДЛП упростит инвентаризацию, а также формирование отчетности. Примеры готовых решений для интеграции с системой маркировки лекарственных препаратов предлагает 1С.
Штрафы за отсутствие маркировки
За нарушение правил реализации товаров, подлежащих обязательной маркировке, российским законодательством предусмотрена ответственность
Подключитесь к системе маркировки самостоятельно
Приобретите 2D-сканер для считывания дата-матрикс кодов, терминал для сбора данных и принтер этикеток.
Обновите прошивку вашей кассы самостоятельно или с помощью наших специалистов.
Получите Квалифицированную электронную подпись для маркировки. Вы можете использовать уже имеющуюся.
Зарегистрируйтесь на сайте Честныйзнак. рф и GS1. Заполните самостоятельно данные о вашем предприятии в личном кабинете или обратитесь к нашим специалистам за помощью!

Получите комплексное предложение по маркировке
Начиная с 2017 года требования к обороту лекарственных препаратов постепенно ужесточались, и в 2020 году в России был принят закон об обязательной маркировке всех лекарств, производимых и реализуемых на территории страны. Как в настоящий момент регистрируются препараты? Приводим пошаговую инструкцию для различных участников рынка.
О чём эта статья
Законодательная основа маркировки.
Участники фармацевтического рынка: — производители; — дистрибьюторы; — аптеки; — медицинские центры
Схема маркирования.
Что представляет собой код маркировки?
Ответственность участников рынка.
Процесс регистрации в системе маркировки. — Аптекам: — что требуется для маркировки; — приёмка препаратов; — продажа товаров в розницу.
Стоматологиям и медицинским центрам: — что необходимо для маркировки; — приёмка; — где взять регистратор выбытия; — списание.
Алгоритм перехода на электронный документооборот
Для перехода на ЭДО нужно пройти следующие этапы:
Этап 1. Выбрать оператора ЭДО и заключить договор
Для работы понадобится усиленная квалифицированная электронная подпись.
Договор можно заключить с любым оператором ЭДО, который участвует в системе Честный ЗНАК. Если вам достаточно обмениваться с контрагентами УПД и УКД по маркированным товарам, можно выбрать бесплатное решение «ЭДО. Лайт» от Честного ЗНАКа, но другие функции там не поддерживаются.
Этап 2. Провести работу с контрагентами
Убедитесь, что все покупатели могут принимать документы по ЭДО. Если такой возможности у них не будет, вы не сможете оформить передачу права собственности. Отправьте контрагентам приглашение к ЭДО и примите приглашения, которые они вам направили.
Бывает, что у контрагентов разные операторы ЭДО. Обмениваться электронными документами это не помешает, но нужно настроить роуминг. Для этого хотя бы один из контрагентов должен подать заявку своему оператору.
Этап 3. Протестировать процессы
Проведите тест документооборота — пройдите с контрагентами полный процесс отгрузки-приемки с оператором ЭДО. Это особенно важно при роуминге.
Если проблемы возникнут после 1 января, когда ЭДО уже будет обязателен, можно не успеть сообщить в Честный ЗНАК о переходе прав собственности и получить штраф.
Не пропустите новые
публикации
Согласно проекту правительства продавать лекарства, не дожидаясь подтверждения маркировки, можно будет до января 2021 года. Мера не коснется препаратов для лечения высокозатратных нозологий

Уведомительный режим работы с маркированными лекарствами будет временно введен для оптово-розничного звена, но не коснется лекарственных препаратов, предназначенных для лечения высокозатратных нозологий (ВЗН). Об этом со ссылкой на проект постановления правительства пишут ТАСС и «Фармвестник». Режим предлагается установить до 1 января 2021 года.
Генеральный директор сети «Ригла» Александр Филиппов, комментируя РБК инициативу правительства, отметил, что в случае лечения ВЗН речь идет не о массовом сегменте продаж лекарств и он обязан контролироваться особым образом. «В нескольких аптеках «Риглы», которые работают с препаратами из списка ВЗН, есть специальные регистраторы выбытия, сложностей с продажами не ожидается», — сказал он.
«Поставки по программе 14 высокозатратных нозологий ожидаются ближе к концу года. Надеемся, что оператор маркировки к этому времени наладит бесперебойную работу системы мониторинга движения лекарственных препаратов», — сообщил в беседе с РБК генеральный директор «Ирвин 2» Михаил Степанов. «Мы со своей стороны всю техническую базу давно подготовили, бизнес-процессы перестроили и в целом выступаем за прозрачность движения лекарственных препаратов на рынке», — уточнил он.

Обязательная маркировка лекарств категории семи высокозатратных нозологий началась 1 октября 2019 года. Для остальных лекарств маркировка стала обязательной с 1 июля. Нововведение направлено на отслеживание каждой упаковки лекарства с момента производства или импорта в Россию до продажи конечному потребителю. Перед вводом маркировки, в марте, Ассоциация российских фармацевтических производителей (АРФП) просила правительство не вводить маркировку из-за неготовности оборудования для маркировки.
24 октября глава Минпромторга Денис Мантуров сообщил о временном переводе системы маркировки лекарств в уведомительный режим работы. В ведомстве связали меру «с недостаточной технической готовностью дистрибьютеров и ряда аптечных организаций к работе с маркированными препаратами». Перед этим в регионах, в том числе в Пермском и Алтайском краях, власти и указывали на уже возникший или скорый дефицит противовирусных и антибактериальных препаратов. В некоторых регионах на отсутствие лекарств в аптеках массово жаловались жители.
Освобождение от маркировки одежды, изготовленной ремесленниками
Распоряжением Правительства РФ от 31. 2021 № 2402-р (далее — Распоряжение № 2402-р, действует с 31. 2021) от обязательной маркировки освобождена одежда и белье, изготовленные ремесленниками. Речь идет о (п. 1-5 Распоряжения № 2402-р):
- предметах одежды, включая рабочую одежду, изготовленных из натуральной или композиционной кожи (код по ОКПД2 — 14.11.10, по ТН ВЭД — 4203 10 000);
- блузках, блузах и блузонах трикотажного машинного или ручного вязания, женских или для девочек (код по ОКПД2 — 14.14.13, по ТН ВЭД — 6106);
- пальто, полупальто, накидках, плащах, куртках (включая лыжные), ветровках, штормовках и аналогичных изделиях (код по ОКПД2 — 14.13.21, 14.13.31, по ТН ВЭД — 6201, 6202);
- белье постельном, столовом, туалетном и кухонном (код по ОКПД2 — 13.92.12, 13.92.13, 13.92.14, по ТН ВЭД — 6302).
Иными словами, ремесленники могут не маркировать всю производимую ими одежду.
Эксперимент по маркировке антисептиков
С 01. 2021 по 31. 2022 в России проводится эксперимент по маркировке антисептиков для рук (Постановление Правительства РФ от 21. 2021 № 1240). Эксперимент касается продукции с кодами:
- ОКПД2 20.20.14.000 и ТН ВЭД ЕАЭС 3808 94 900 0 — в части кожных антисептиков — дезинфицирующих средств;
- ОКПД2 20.42.15 и ТН ВЭД ЕАЭС 3304 99 000 0 — в части парфюмерно-косметической продукции, предназначенной для гигиены рук, с заявленным в маркировке потребительской тары антимикробным действием.
Организации и предприниматели принимают участие в эксперименте добровольно. Для участия в эксперименте необходимо направить заявку в ИС МП «Честный знак». Зарегистрированные участники эксперимента смогут принимать участие в рабочих группах, получат доступ к технической документации и личному кабинету, а также поддержку по настройке процесса нанесения кодов и других бизнес-процессов.
Отметим, что в настоящее время также проводятся эксперименты по маркировке:
- биологически активных добавок (БАД) к пище — с 01.05.2021 по 31.08.2022 (Постановление Правительства РФ от 29.04.2021 № 673);
- пива и слабоалкогольных напитков — с 01.04.2021 по 31.08.2022 (Постановление Правительства РФ от 17.02.2021 № 204).
Новые сроки выдачи лицензии производителям
Министерство промышленности и торговли предложило изменить сроки выдачи лицензий на производство лекарственных средств. Дело в том, что с сентября, когда вступит в силу новое положение о лицензировании фармацевтической деятельности, максимальный срок будет составлять 15 дней.
В министерстве сразу предупреждают, что не смогут выполнить это требование, поскольку штат Департамента развития фармацевтической и медицинской промышленности, который занимается выдачей лицензий, составляет всего десять человек.
Учитывая, что для выдачи лицензии необходима выездная инспекция производственных площадок, которых у компании может быть несколько, у ведомства просто не хватит сотрудников. Кром этого, в проекте документа сказано, что на сроки выдачи лицензии может повлиять «необходимость оперативного решения задач, связанных с текущими эпидемиологической и политической ситуациями».
В связи с этим Минпромторг предлагает установить максимальный срок выдачи лицензии в 30 рабочих дней, с возможностью его увеличения на 10 или 15 дней в зависимости от количества адресов осуществления деятельности, указанных в заявке лицензиата.
Следует отметить, что даже в случае принятия документа, он начнёт действовать не ранее 1 марта 2023 года. Таким образом, в течение, как минимум, полугода Минпромторгу придётся как‑то успевать оформлять лицензии в течение 15 дней.
Работайте с нами
Наши специалисты проведут подключение маркировки «под ключ»: вам нужно будет только начать работать! Настройка, регистрация, запуск, обучение — доверьте все нашим профессионалам.
Выгодно
Гибкая ценовая политика, предложения и скидки для новых и постоянных клиентов. Мы предоставляем возможность приобрести все необходимое для маркировки в одном месте по оптимальной стоимости.
Квалифицированные специалисты, собственный склад — вам не придется ждать.
Быстро
Проводим подключение силами собственных квалифицированных специалистов и с оборудованием, находящимся на собственном складе — вам не придется ждать.
Удобно
Мы предлагаем комплексный подход к обязательной маркировке: оборудование, ПО и сопровождение от А до Я. Все для маркировки в одном месте «под ключ» быстро и качественно!
Видео
Оборот лекарственных препаратов на территории России строго контролируется. Все производители, дистрибьюторы, продавцы (аптеки) и прямые потребители, получающие препараты по контрактам (например, стоматологии, поликлиники и т. ), регистрируются в единой системе МДЛП, где каждый из участников занимает свою нишу. Из-за жёсткого мониторинга внедрение в данную иерархию несанкционированных компаний весьма затруднено.
Участники рынка обязаны учитывать маркировку продукции, однако делают это в пределах своей компетенции и в установленном порядке. Работа по регистрации препаратов и их перемещению осуществляется онлайн только зарегистрированными в системе пользователями. В постановлениях № 1556 и № 1557 подробно перечислены обязанности и алгоритм действия участников фармацевтического рынка РФ.
Производители
Первыми наносят маркировку (код) на упаковку при изготовлении лекарств, при этом обязательно регистрируют новый препарат на сайте МДЛП как впервые вводимый в обращение.
Дистрибьюторы
Логистические комплексы и дистрибьюторские компании, которые производят расформирование оптовых партий лекарств, фармацевтическую продукцию не маркируют, но отчитываются о движении товаров, направляя информацию в систему МДЛП: при получении лекарственных препаратов на склад, при расформировании оптовых упаковок, при отгрузке товаров со склада.
Аптеки
Направляют данные о прибытии лекарственных препаратов на аптечный склад и об их оприходовании. А также отчитываются о приобретении препаратов через онлайн-кассу и при выбытии товаров из оборота с указанием причины.
Регламентированные причины выбытия препаратов из оборота – это реализация, утеря (недостача), списание бракованных товаров, частичное списание недоукомплектованных упаковок или товаров, утилизация, списание товаров без утилизации.
Медицинские центры
Направляют отчёт в систему МДЛП при приёме лекарственных препаратов на склад, при внутреннем движении (например, со склада в отделение), при списании по причине оказания медицинских услуг (прямое применение лекарств в условиях стационара), при выбытии из обращения с указанием причин.
Уведомительный режим маркировки может стать бессрочным
7 декабря 2021

Министерство промышленности и торговли предложило законодательно закрепить возможность использования «уведомительного» режима системы маркировки лекарственных средств. Проект соответствующего постановления опубликован на портале нормативных актов.
Напомним, что 1 февраля 2022 года истекает срок действия поправки, которая разрешает аптекам при приёмке ЛС не дожидаться от поставщиков дополнительного подтверждения передачи в ГИС МДЛП необходимой информации (схема 702). Такие данные автоматически подтверждает сам оператор.
Минпромторг предлагает добавить в Положение о системе мониторинга движения лекарственных препаратов изменение, которое навсегда закрепит возможность использования такой схемы приёмки ЛС.
«Уведомительный» режим работы с маркировкой был введён после масштабного сбоя в работе системы в сентябре прошлого года. Тогда из‑за технической неисправности были потеряны данные об уже загруженных в систему маркировки препаратах. Data Matrix коды не считывались, из‑за чего в системе невозможно было отразить передачу препаратов — производители и дистрибьюторы не могли поставить товар на продажу, а аптеки не могли его принять.
Изначально предполагалось, что упрощённой схемой приёмки ЛС можно будет пользоваться до 1 июля 2021 года, однако позже Правительство продлило действие этого режима до февраля 2022 года.
Без чего не обойтись предпринимателям при торговле маркированными лекарственными препаратами
Аптекам для продажи маркированных лекарственных препаратов не обойтись без специального оборудования:
В связи с обязательной маркировкой товаров в России в 2021 году введены: с 1 августа – новый формат фискальных документов ФФД 1. 2, а с 6 августа – новая модель фискального накопителя ФН-1.
ФФД 1. формирует тег для маркировки в чеке – 1163 «код товара».
Реестр ККТ, поддерживающей ФФД 1. 2 и Реестр ФН опубликованы на сайте ФНС.
Что делать, если кассовый аппарат у вас уже есть:
- Касса куплена до 01.08.2021 года, установленный ФН не поддерживает ФФД 1.2 – продолжайте работать на старом фискальном накопителе до конца срока его действия. По окончании срока проверьте наличие кассы в Реестре ККТ. Если она там есть, необходимо будет обновить ПО кассы, приобрести новый ФН-1.1М и перерегистрировать кассу с новым ФН в Налоговой. Если нет – кассу придется менять.
- Касса приобретена до 01.02.2022, касса и ФН поддерживают ФФД 1.2 – необходимо перейти на новый формат не позднее 3-х месяцев с даты внесения кассы в Реестр ККТ.
- Касса приобретена 01.02.2022 или позже – работать на ФФД 1.2 нужно сразу.
Кассу не обязательно покупать. Вы всегда можете взять кассу напрокат.
Если вам предстоит покупка новой ККТ, сначала выберите кассу, а потом подберите к ней подходящий сканер, т. не вся техника совмещается друг с другом.
Также советуем обратить внимание на онлайн-кассы со встроенным 2D-сканером.
Для маркировки идеально подходит МТС Касса 5 PRO. Это новая прокачанная модель на рынке онлайн-касс. Вместо обычной камеры с функцией сканирования, здесь встроен полноценный матричный имидж-сканер. Он в десятки раз быстрее считывает коды любой сложности (за 0,1 секунды), распознает потертые и изогнутые изображения, работает даже в полной темноте. В отличие от простой камеры, сканер не имеет технических ограничений и улавливает коды на расстоянии до 30 см и под углом до 45°.
Также аптечным пунктам понадобится обязательная квалифицированная электронная подпись для регистрации и работы в ИС МДЛП и ЭДО.
С 1 января 2022 года для юридических лиц (руководителей), ИП и нотариусов ФНС изготавливает бесплатные КЭП. Получить подписи можно только в удостоверяющих центрах ФНС России.
О том, как получить бесплатную КЭП через налоговую службу мы подробно писали здесь.
Штрафы до 300 000 ₽ за лекарства без маркировки
С 1 июля 2020 года маркировка лекарств станет обязательной, а значит, будут штрафы.
Штрафы за производство лекарств без маркировки:
- для ИП — от 5000 до 10 000 рублей;
- для компаний — от 50 000 до 100 000 рублей.
За продажу и выдачу лекарств без маркировки:
- для ИП — от 2000 до 4000 рублей;
- для компаний — от 50 000 до 300 000 рублей.
Если выявят нарушение, оштрафуют и конфискуют немаркированные лекарства. Исключение — лекарства, которые были выпущены без маркировки до 1 июля 2020 года, — их можно продавать до конца срока годности.
Питание для спортсменов и бытовая химия в аптеках
Безусловно самым главным событием в июне стало предложение депутатов Государственной думы расширить ассортимент товаров, которые можно продавать в аптеках. Законопроект был внесён в Думу в начале месяца.
Таким образом депутаты хотят дать аптекам дополнительные источники заработка в текущей не очень стабильной экономической ситуации. В перечень вошли 18 видов товаров:
Пока документ не прошёл ни одного чтения. Поэтому точная дата, когда в аптеку можно будет зайти за термобельем и жевательной резинкой, пока не определена.
Обязательный ЭДО в маркировке молочной продукции
С 1 сентября 2022 года участники маркировки молока и молочной продукции должны перейти на электронный документооборот. Требование относится к производителям, импортерам, оптовикам и розничным продавцам. Им необходимо подключиться к сервису ЭДО и начать вести объемно-сортовой учет (ОСУ). Это упрощенный вариант передачи сведений о маркировке в Честный ЗНАК. Его отличие в том, что не нужно отправлять данные о перемещении каждой единицы товара, учитываются партии молочной продукции. Для этого в электронных УПД указываются только наименование (код GTIN) и количество товара, а индивидуальные коды маркировки заносить не нужно.
Правила действуют для товаров:
- молоко и сливки, кроме сырых;
- сгущенные молоко и сливки с сахаром;
- сливочное масло, в том числе топленое;
- спреды и смеси сливочно-растительные;
- кисломолочные продукты, в том числе йогурт, кефир;
- мороженое, пищевой лед;
- безалкогольные напитки с содержанием молочного жира.
Перенесли сроки маркировки для фермерских хозяйств, общепита и госучреждений — они начнут подавать сведения об обороте молока и молочной продукции в Честный ЗНАК с 1 декабря 2023 года, все остальные организации должны быть готовы к изменениям с 1 сентября 2022 года.
Процесс регистрации в системе маркировки
Юрлицам и индивидуальным предпринимателям для регистрации требуется усиленная ЭЦП (электронно-цифровая подпись). Для работы в системе следует установить плагин «КриптоПро» и СКЗИ с подтверждённым сертификатом. При открытии диалогового окна необходимо указать данные сертификата УКЭП, при этом информация о пользователе загрузится автоматически. Затем нужно добавить данные лицензии и закончить регистрацию, поставив ЭЦП. Ваше заявление будет рассмотрено в течение 10 рабочих дней.
Применение 1С-ЭДО при операциях с маркированными товарами
По общему правилу участники маркированного товарооборота при приеме и отгрузке продукции передают в государственную систему маркировки информацию о переходе права собственности на товар в электронном виде.
В настоящее время электронный документооборот (ЭДО) обязателен для табачной продукции (Постановление Правительства от 28. 2019 № 224). Универсальные передаточные документы (УПД) или универсальные корректировочные документы (УКД), которыми оформляется оборот маркированных товаров, представляются в ИС МП «Честный знак» самостоятельно участником оборота (через личный кабинет ИС МП) или после его получения оператором электронного документооборота.
С 01. 2022 обязательным становится использование ЭДО при оптовой торговле в товарных категориях: шины, фототовары, духи и туалетная вода, обувная продукция, легкая промышленность.
Обратите внимание, если молочная продукция, подлежащая маркировке, приобретена организациями для собственных нужд (например, ресторанами, кафе, детскими садами, школьными столовыми, больницами и пр. ), то такие компании становятся участниками оборота маркируемых товаров, должны передавать сведения о маркировке молочной продукции в ИС МП и использовать ЭДО: оформлять приобретение такой продукции с помощью электронного УПД (УКД) и осуществлять вывод из оборота молочной продукции с указанием причины, не связанной с последующей реализацией (для собственных нужд).
Передать данные в составе УПД (УКД) с 01. 2022 можно будет только через оператора ЭДО. Возможность представления УПД (УКД) через личный кабинет ИС МП отменяется (Постановление Правительства РФ от 31. 2020 № 2464). Для этого участнику оборота маркированных товаров необходимо подключиться к электронному документообороту через оператора ЭДО. Если вы этого еще не сделали, рекомендуем заблаговременно подготовиться к новым правилам работы. В программах 1С для обмена электронными документами с контрагентами применяется встроенный сервис 1С-ЭДО.
Подробнее о том, как подключиться к 1С-ЭДО (доступна видеоинструкция).
Быстро и легко освоить 1С-ЭДО можно с помощью видеороликов — см. на сайте 1С-ЭДО в разделе «Техподдержка» и на Youtube-канале 1С:Учебного центра № 1. Плей-лист с роликами 1С-ЭДО см. на Youtube-канале.
Также если пользователь 1С-ЭДО только начинает знакомство с сервисом, то в освоении функционала и решении возникших вопросов помогут контекстные советы-подсказки.
Помогут начать работу с маркированными товарами партнеры 1С.
По всей стране по единой специальной цене партнеры 1С оказывают комплекс услуг по запуску в продажу маркированного товара:
- подключение к системе электронного документооборота (1С-ЭДО);
- регистрация в национальном каталоге GS1;
- создание или обновление справочника номенклатуры;
- обучение пользователей работе с маркированным товаром;
- подключение и настройка торгового оборудования;
- настройка программы 1С для работы с маркированным товаром.
Узнать подробнее можно на сайте «1С» для эффективной торговли.
Ответственность участников рынка
Нарушение законодательства в процессе производства и продажи лекарственных препаратов, а также допуск препаратов в торговую сеть без обязательной маркировки влечёт административную и уголовную ответственность.
Если общая стоимость немаркированных товаров, допущенных в оборот, составляет менее 1 500 000 рублей, то ответственное лицо наказывается денежным штрафом:
- индивидуальные предприниматели − 5−10 тысяч рублей;
- юрлица − 50−300 тысяч рублей.
Уголовному преследованию подвергаются недобросовестные и несанкционированные участники рынка, которые допустили к реализации немаркированные контрафактные или поддельные лекарства на сумму более 1 500 000 рублей. Согласно законодательству Российской Федерации, ответственное лицо ждёт реальный тюремный срок до 3 лет и штраф в размере 80 тысяч рублей.
С полным перечнем нарушений и санкций можно ознакомиться на сайте «Честный знак».

В России упростили систему маркировки лекарств из-за повышенного спроса
Аптеки смогут продавать лекарства, не дожидаясь подтверждения от системы о том, что сведения о приемке успешно зарегистрированы. Мера позволит ускорить движение препаратов на фоне повышенного спроса и пандемии, указывает кабмин

Премьер-министр Михаил Мишустин подписал постановление, которое упрощает порядок работы с системой маркировки лекарств, сообщается на сайте правительства.
«Учитывая повышенный спрос на лекарства и эпидемиологическую ситуацию, упрощенный режим будет функционировать до полной готовности всех участников отрасли», — говорится в сообщении.
Согласно упрощенному режиму, аптеки и медучреждения смогут выводить лекарства из оборота через кассы сразу после уведомления системы о поступивших к ним препаратах и не ждать подтверждения от системы, что сведения о приемке успешно зарегистрированы.
До 1 июля следующего года также вводятся упрощенные механизмы «обратной приемки лекарств» при их ввозе в Россию и обороте внутри страны. При таком режиме участники смогут не дожидаться от поставщиков подтверждения приемки препаратов. Аналогично при ввозе лекарств в Россию импортеры могут не ждать от держателей или владельцев регистрационного удостоверения на препараты подтверждения ввоза. Эти сведения будут автоматически подтверждаться самой системой путем проверки кода товара и данных участника.
Упрощенный режим маркировки распространяется на все лекарства, за исключением лекарств из категории 12 высокозатратных нозологий.

В ЦРПТ (оператор маркировки) сообщили ТАСС, что из-за возросшего спроса на лекарства и пандемии решили выдавать и прослеживать коды на все лекарства, произведенные с ноября 2020 года до февраля 2021 года, бесплатно. Это поможет упростить бизнес-процессы и снизить нагрузку на отрасль, указали в ЦРПТ.
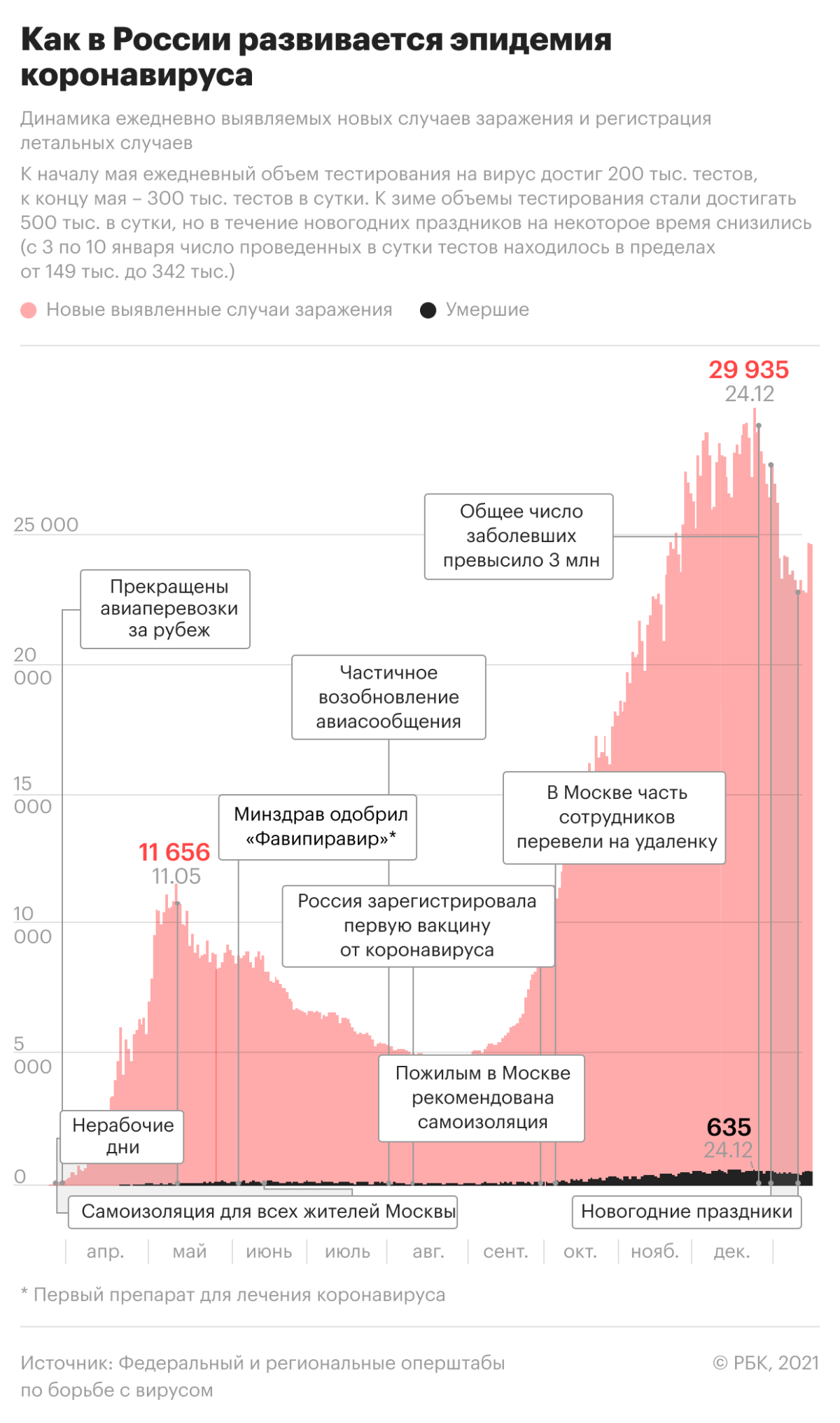
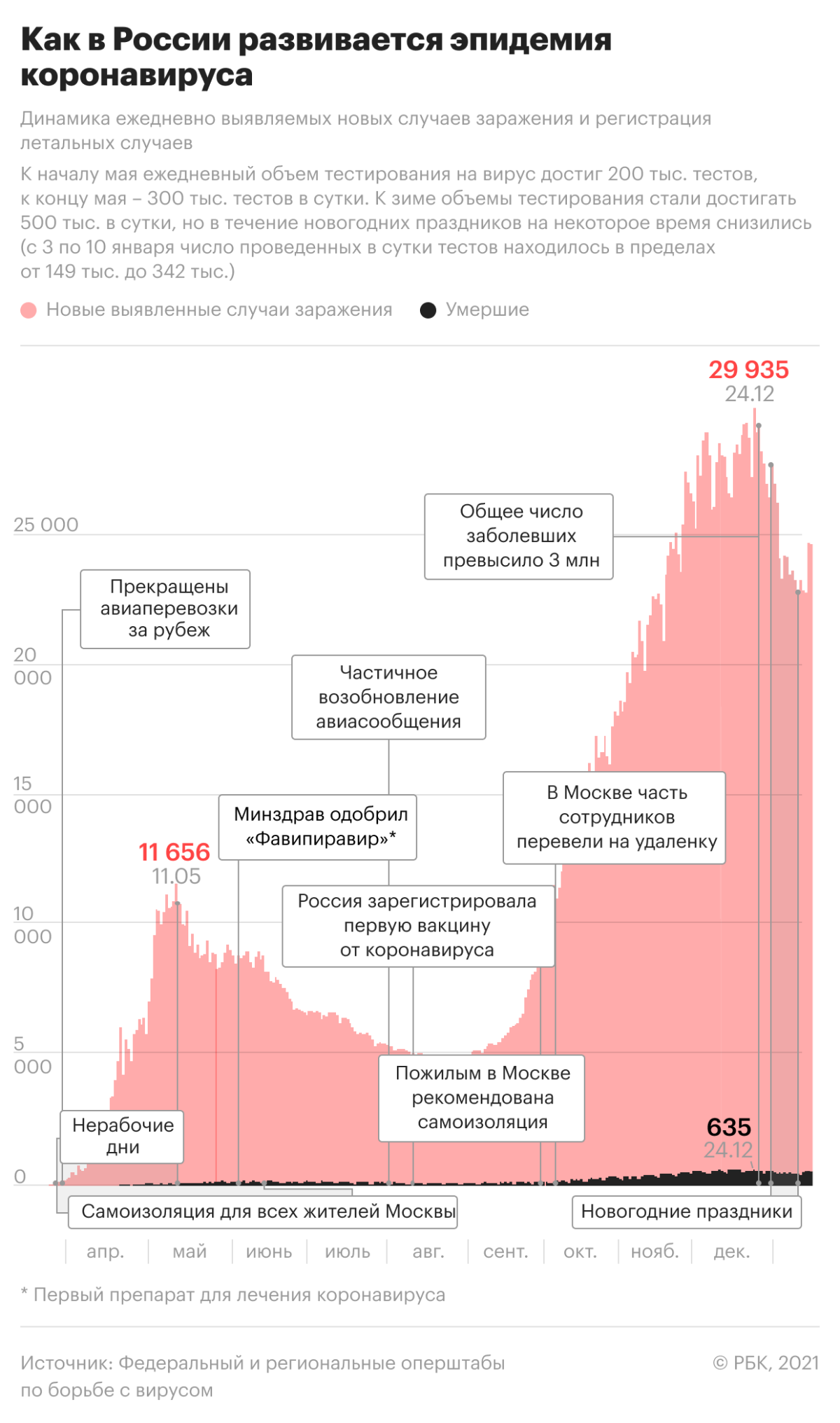
В октябре в нескольких российских регионах, в том числе в Омской области и Республике Алтай, возник дефицит противовирусных лекарств. В Москве и Подмосковье в конце месяца из продажи пропал жизненно важный антикоагулянт «Клексан», который применяется в том числе для лечения COVID-19. В некоторых случаях аптеки не могли продать лекарства, несмотря на их наличие: система маркировки находилась в режиме обновления или фиксировался сбой. В Ассоциации международных фармацевтических производителей (AIPM) сообщали, что из-за проблем с системой маркировки в розницу не могут быть своевременно поставлены 40 млн упаковок более 450 различных препаратов.
Маркировка всех лекарств стала обязательной в России с 1 июля. С 1 октября 2019 года она была обязательной только для лекарств, предназначенных для лечения по программе высокозатратных нозологий. Цель маркировки — проследить каждую упаковку лекарства от момента производства или импорта в Россию до продажи конечному покупателю.
Отсрочка обязательной маркировки велосипедов
До 01. 2022 отсрочили обязательную маркировку велосипедов (в том числе со вспомогательным двигателем и трехколесных) и велосипедных рам (п. 6 Распоряжения № 2402-р). Напомним, что ранее в соответствии с Распоряжением Правительства РФ от 28. 2018 № 792-р введение обязательной маркировки таких товаров было запланировано на 01. 2021.
Маркировка лекарств в 2021 году
Обязательная маркировка лекарственных препаратов вводится с 1 июля 2020 года. С этого дня все лекарства должны иметь на своей упаковке средства идентификации, а сведения о них необходимо передавать в систему «Честный ЗНАК» на каждом этапе оборота. Первое звено в этой цепочке — производитель. Расскажем, как подготовить производство к обязательной маркировке лекарств.
Этапы и порядок подготовки установлены Постановлением Правительства РФ №1556 и №1118. До начала обязательной маркировки ЛС необходимо сделать следующее:
- С 1 января до 29 февраля 2020 года все участники оборота лекарств должны были пройти регистрацию в системе маркировки.
- До 15 февраля 2020 года медицинские учреждения и аптеки должны были подать заявку на получение регистратора выбытия.
- До 1 мая 2020 года производители и импортеры лекарств обязаны подать заявку на получение регистратора эмиссии.
- С 1 июля 2020 года все участники оборота должны передавать сведения о движении лекарств в систему маркировки.
Для соблюдения требований к маркировке лекарственных средств производителям нужно было подготовить свои рабочие места: приобрести необходимое оборудование и установить программное обеспечение. До 1 июля 2020 года производители имели право не маркировать лекарства. Такие препараты участвовали в обороте до истечения срока годности. Однако из-за пандемии и повышенного спроса на лекарства в этот период многие участники оборота ЛС не успели подготовиться. Некоторые фармкомпании просили о переносе сроков маркировке лекарства на 2021 год. В связи с этим Правительство ввело некоторые послабления. Аптекам разрешили по согласованию с Росздравнадзором реализовывать без маркировки лекарственные препараты, произведённые в период с 1 июля по 1 октября 2020 года.
С Постановлением Правительства № 1779 до 1 июля действуют следующие послабления:
- аптеки и медицинские учреждения могут выводить ЛС из оборота сразу после передачи в «Честный ЗНАК» информации об их поступлении;
- участники оборота ЛС могут оприходовать лекарства и проводить с ними дальнейшие операции, не дожидаясь от поставщиков подтверждения приёмки;
- импортёры могут не ждать подтверждения ввоза ЛС на территорию РФ.
Какие лекарства подлежат маркировке
Эксперимент по маркировке лекарств начался в 2017 году. Согласно Федеральному закону № 61-ФЗ, с 1 июля 2020 года обязательная маркировка ЛС распространяется на все препараты, произведённые или ввозимые на территорию РФ.
Как производителю работать с маркировкой
Производитель обязан наносить на каждую потребительскую упаковку уникальный двумерный код Data Matrix. Этот код содержит информацию о препарате:
- серийный номер мед. препарата (GTIN) и номер партии;
- идентификатор ключа и код проверки криптозащиты (ГОСТ 34.10-2012).
Помимо этого, при необходимости он может содержать наименование препарата и производителя, срок годности лекарства, инструкцию по использованию и другую информацию.
Получение кода Data Matrix
Прежде чем получить коды для каждой упаковки, необходимо описать лекарственные препараты, которые выпускает производитель. Для этого ему нужно:
Для защиты потребителей от контрафакта Правительство РФ приняло решение взять под государственный контроль всю продукцию, которая производится в России и импортируется на территорию страны. Для этого с 2019 вводится повсеместная обязательная маркировка товаров. К 2024 году каждая единица будет иметь уникальную метку.
Внести информацию о производимых лекарствах и указать, что ЛС участвует в проекте по маркировке.
Подать заявку на генерацию кодов в «Личном кабинете» ИС МДЛП.
Производитель может выбрать размер кода в зависимости от габаритов упаковки: 10х10, 12х12 или 16х16 мм. Помимо этого, он может запросить коды на несколько месяцев или на год вперёд, а также сгенерировать коды сразу на несколько производственных площадок.
Нанесение кода Data Matrix на упаковку
Далее производитель печатает коды с помощью принтера этикеток и наклеивает на каждую потребительскую упаковку. После этого необходимо сообщить в ИС МДЛП:
- дату операции;
- данные производителя-фасовщика и собственника товара, если лекарства производят по договору;
- срок годности препарата;
- перечень использованных кодов Data Matrix.
Если партию препаратов помещают в транспортную упаковку, то на неё наносят коды формата GS1 128. Такой код содержит данные обо всех упаковках внутри. После нанесения средств идентификации необходимо передать в ИС МДЛП:
- дату совершения операции;
- данные фасовщика;
- перечень кодов агрегации, к каждому из которых нужно указать перечень вложенных кодов.
Комментарий эксперта Евгения Мео.
Эти данные нужно подать в течение 5 дней после агрегации, но до совершения других операций с товаром.
Контроль качества и запуск лекарства в оборот
Прежде чем пускать лекарство в оборот, необходимо отобрать контрольные и архивные образцы и отправить на экспертизу предприятию, которое занимается контролем качества лекарственных препаратов. Об этом также нужно сообщить в ИС МДЛП. Если качество препарата соответствует установленным требованиям, производитель получит соответствующее подтверждение и сможет ввести продукцию в оборот, передав сведения об этом в систему мониторинга.
Получить усиленную квалифицированную электронную подпись.
Установить СКЗИ для работы с УКЭП.
Заключить договор с оператором ЭДО.
Заполнить профиль организации в личном кабинете системы.
Приобрести принтер этикеток и 2D-сканер.
Подготовить производство и установить оборудование, необходимого для связи с ИС МДЛП и регистратором эмиссии.
Установить программно-аппаратный комплекс: регистратор эмиссии и систему управления заказами.

Как происходит процесс оборота лекарств
Обязательная маркировка лекарств повлияла на работу производителей, импортеров, продавцов, медучреждений и тех, кто занимается уничтожением испорченных и просроченных медикаментов. Теперь каждая упаковка лекарственных средств должна быть промаркирована.
Чтобы продавать лекарства в соответствии с новыми правилами, необходимо знать, как работает система и применять оборудование, которое может работать с маркировкой лекарств и осуществлять передачу данных о перемещении лекарственных товаров в онлайн-систему.
Маркировка лекарственных средств осуществляется при помощи нанесения на каждую упаковку препарата, поступающего в розничную продажу, а также на транспортировочную тару специальных кодов маркировки Data Matrix. Код генерируется и присваивается каждому препарату производителем.
Для того чтобы отследить движение препаратов от производителей до конечного пользователя или утилизации установлены правила работы в инфосистеме. Они предполагают наличие простого алгоритма, который и делает систему эффективной и прозрачной:
- Ввод лекарств в оборот. Производители (импортеры) специальным оборудованием генерируют и наносят на упаковки двухмерный штрихкод. Для этого требуется специальное оборудование для маркировки лекарств. Затем регистрируют выпуск препарата в ИС МДЛП с указанием уникальных идентификаторов.
- Отгрузка. Сведения в ИС МДЛП о поступлении лекарственных препаратов от производителей (импортеров) оптовикам, рознице или в больницы, а также от оптовиков рознице, можно фиксировать в прямом и обратном порядке.
Прямой ─ информация о поставке маркированной продукции поступает в инфосистему от отправителя, а получатель должен ее подтвердить.Обратный ─ данные в ИС МДЛП направляет получающая сторона, а проверяет поставщик. - Прямой ─ информация о поставке маркированной продукции поступает в инфосистему от отправителя, а получатель должен ее подтвердить.
- Обратный ─ данные в ИС МДЛП направляет получающая сторона, а проверяет поставщик.
- Работа построена на обмене EDI-сообщениями: «Заказ» и «Ответ на заказ», плюс универсальными передаточными документами (УПД), заверенными усиленными квалифицированными электронными подписями через платформу ЭДО.
- Способ работы с документами выбирают отправитель и получатель. Так, маркировка позволит фиксировать движение каждой упаковки лекарственной продукции быстро и точно.
- Вывод лекарств из оборота. Сведения о розничной продаже, выдаче по льготному рецепту, расходе на лечение в больнице, передаче на уничтожение собранные по маркерам на упаковках передаются в ИС МДЛП (регистратор выбытия).
- При продаже обязательной является отправка в инфосистему данных о дате, кассовом чеке, стоимости и уникальных идентификаторах с упаковки. В тех случаях, когда аптеки выдают лекарства по льготному рецепту, в ИС МДЛП нужно передать информацию и о его реквизитах.
- После поступления в инфосистему сведений о выводе товара, проданные, выданные на лечение и переданные на утилизацию лекарства и их идентификаторы, указанные на упаковке, списываются.
Управлять и отслеживать учет и движение маркированных лекарственных средств можно в личном кабинете пользователя системы.






